Articles
- Page Path
- HOME > J Musculoskelet Trauma > Volume 34(4); 2021 > Article
- Review Article Romosozumab: A Novel Agent in the Management of Osteoporosis
- Nam Hoon Moon, Won Chul Shin, Jae Hoon Jang
-
Journal of Musculoskeletal Trauma 2021;34(4):148-153.
DOI: https://doi.org/10.12671/jkfs.2021.34.4.148
Published online: October 31, 2021
2Department of Orthopaedic Surgery, Pusan National University Yangsan Hospital, Yangsan, Korea
- 1,319 Views
- 11 Download
- 2 Crossref
- 0 Scopus
Abstract
With the discovery of screlostin as a pivotal player in bone metabolism, a novel medication targeting sclerostin has been introduced. Romosozumab, a humanized anti-sclerostin monoclonal antibody, is a unique approach to the treatment of osteoporosis that inhibits sclerostin, a key regulator that has the dual properties of promoting bone formation and inhibiting bone resorption. Romosozumab has been shown to be superior to conventional agents, in increasing bone mineral density and preventing osteoporotic fractures. Romosozumab may also be effective in the management of treatment-resistant osteoporosis and in the prevention of osteoporotic fractures in the very high risk population. However, further studies are necessary as there is insufficient data on its clinical efficacy and safety.
Published online Oct 25, 2021.
https://doi.org/10.12671/jkfs.2021.34.4.148
초록
과도한 골형성을 보이는 유전 질환의 병인에 대한 연구를 통해 골대사에 sclerostin이 중요한 역할을 한다는 것이 밝혀진 후, 이를 이용한 새로운 골다공증 치료제가 제시되었다. 로모소주맙은 인간화 항-sclerostin 단클론 항체로 골대사에 중요한 조절 인자인 sclerostin을 억제하여 골형성 촉진, 골흡수 억제 등 이중 작용 기전을 가지는 새로운 골다공증 치료제이다. 로모소주맙은 기존 골다공증 치료제의 단점을 보완하고, 이들에 비해 골밀도 증가, 골절 예방에서 우수한 효과를 가진다고 현재까지 보고되고 있다. 또한 지속적인 치료에도 반응하지 않는 골다공증, 초고위험군에서의 치료에서도 좋은 결과를 보일 것으로 기대되고 있다. 그러나 아직 임상 효과, 부작용 등에 대한 결과가 충분하지 않은 실정으로 이에 대한 지속적인 추가 연구가 필요할 것으로 생각된다.
Abstract
With the discovery of screlostin as a pivotal player in bone metabolism, a novel medication targeting sclerostin has been introduced. Romosozumab, a humanized anti-sclerostin monoclonal antibody, is a unique approach to the treatment of osteoporosis that inhibits sclerostin, a key regulator that has the dual properties of promoting bone formation and inhibiting bone resorption. Romosozumab has been shown to be superior to conventional agents, in increasing bone mineral density and preventing osteoporotic fractures. Romosozumab may also be effective in the management of treatment-resistant osteoporosis and in the prevention of osteoporotic fractures in the very high risk population. However, further studies are necessary as there is insufficient data on its clinical efficacy and safety.
서 론
세계보건기구(World Health Organization, WHO)에서는 골다공증을 골량의 감소와 미세구조의 이상을 특징으로 하는 전신적인 골격계 질환으로 뼈가 약해져서 부러지기 쉬운 상태로 정의하고 있다. 우리나라는 2017년을 기준으로 65세 이상 인구가 전체 인구의 14%를 넘어서는 고령 사회에 진입하였고 현재는 매우 빠른 속도로 초고령 사회의 진입을 눈앞에 두고 있다. 이에 고령 인구의 삶의 질에 직접적인 연관이 있는 골다공증에 대한 예방과 치료의 중요성은 점점 더 커지고 있다.
현재 사용 중인 골다공증 치료제는 크게 선택적 에스트로겐 수용체 조절제(selective estrogen receptor modulator, SERM), 비스포스포네이트(bisphosphonate), 데노수맙 (denosumab) 등의 골흡수 억제제와, 부갑상선호르몬 제제 (parathyroid hormone, PTH)와 같은 골형성 촉진제로 구분될 수 있다. 이러한 기존의 골다공증 치료제에 더해 최근 새로운 골형성 촉진제인 로모소주맙(romosozumab)이 많은 관심을 받고 있다. 로모소주맙은 Wnt 단백질을 억제하는 sclerostin 단백질에 대한 단클론 항체(monoclonal antibody)로 2019년 4월에 미국 식품의약국(U.S. Food and Drug Administration, FDA)의 승인 후 현재 우리나라에서도 사용중에 있다. 이 약제의 주요 작용 기전은 골대사에 중요한 조절인자 중 하나인 sclerostin을 억제하여 골형성은 촉진시키고 일시적으로 골흡수를 억제시키는 등의 이중 효과를 보인다는 것이다.1,2) 이를 통해 골밀도의 증가와 골절 예방 효과가 기존의 약제에 비해 우수할 것이라는 이론적 배경을 바탕으로 많은 임상 의사들의 기대를 받고 있다. 이에 저자들은 현재까지의 보고들을 바탕으로 로모소주맙의 작용 기전, 임상 효과 및 안전성에 대해 기술하고 새로운 골다공증 치료제로서의 역할에 대해 알아보고자 한다.
본 론
1. 로모소주맙의 작용 기전과 이중 효과
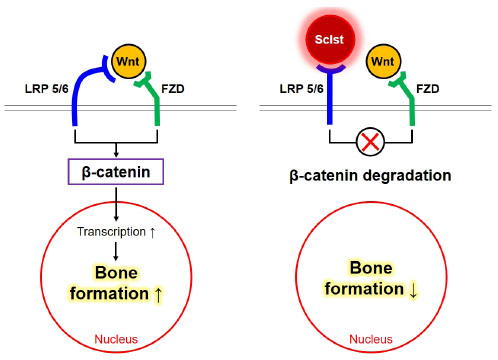
Sclerostiosis와 Van Buchem disease는 과도한 골형성을 보이는 상염색체 열성 유전 질병으로, 그 병인에 대한 연구에서 sclerostin이 골형성에 중요한 조절 인자로 작용한다는 것이 밝혀졌다.3) Wnt 단백질은 골모세포의 세포막에서 low-density lipoprotein receptor-related protein 5 or 6 (LRP 5/6) 복합체와 Wnt-Frizzled (FZD)의 결합을 통해 β-catenin의 신호 전달을 활성화시키고, 그 결과 골형성과 관련한 골기질 단백질을 만들어내거나 이와 관련된 세포들을 분화시켜 골형성을 촉진하게 된다.4,5) 이러한 과정 중 sclerostin은 LRP5/6 복합체에 결합하여 Wnt-FZD와의 결합을 방해하게 되어 Wnt/β-catenin 신호 전달이 억제되고, 이로 인해 골형성이 억제되게 된다.6) 즉, 로모소주맙은 골형성에 중요한 Wnt/β-catenin 신호 전달을 억제하는 sclerostin을 억제하여 골형성을 촉진하게 된다(Fig. 1).
Fig. 1
Wnt/β-catenin signaling pathway and sclerostin. LRP 5/6: low-density lipoprotein receptor-related protein 5 or 6, FZD: Frizzled, Sclst: sclerostin.
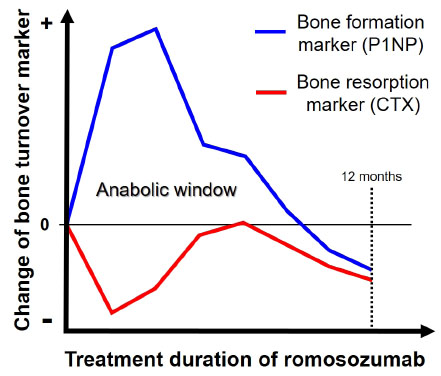
또한 sclerostin은 골흡수에 대한 간접 자극제로서의 기능을 한다. Wnt 신호 전달 체계의 활성은 RANK ligand (RANKL)의 작용을 억제하는 osteoprotegerin (OPG)의 발현을 촉진하는데, sclerostin은 OPG를 감소시키고 RANKL의 작용을 유도하여 골흡수를 촉진하게 된다. 따라서 sclerostin의 기능을 억제하는 로모소주맙은 RANKL/OPG의 비율을 감소시켜 골흡수를 억제하는 효과를 갖는다.7) 이와 같이 로모소주맙은 sclerostin의 억제를 통해 골형성 촉진과 골흡수 억제를 동시에 가지게 되는데, 이를 이중 작용 효과라고 하며, 이는 로모소주맙을 투여받은 연구 대상자들의 골형성 표지자 procollagen type 1 N-terminal propeptide (P1NP)와 골흡수 표지자 C-terminal telopeptide of type I collagen (CTX)의 체내 변화를 통해 확인된 바 있다(Fig. 2).8,9,10)
Fig. 2
Anabolic window for romosozumab.
2. 로모소주맙의 약력학과 약동학
건강한 성인을 대상으로 한 초기 연구에서 로모소주맙의 1회 피하 또는 혈관주사는 P1NP, bone alkaline phosphate (BAP), osteocalcin과 같은 골형성 표지자의 유의한 증가와 CTX와 같은 골흡수 표지자의 완만한 감소를 보여주었다. 이러한 변화는 용량에 의존적이며, 골흡수 표지자가 약 50%가량 감소할 때 골형성 표지자는 약 두 배가량 증가하는 양상을 보였다.11) 골감소증이 있는 폐경기 여성 및 남성을 대상으로한 연구에서는 로모소주맙을 투여한 후 초기 8주 동안 P1NP의 상승이 나타났는데, 여성에서는 2 mg/kg을 2주마다 투여하였을 때, 남성에서는 3 mg/kg을 4주마다 투여하였을 때 가장 큰 반응이 나타났다.12) McClung 등13)의 폐경기 여성을 대상으로 한 로모소주맙의 효과에 대한 비교연구에서 P1NP의 증가가 약물 투여 후 1주일부터 나타나기 시작하여 1개월이 되었을 때 최대치가 되었고 29개월 후에 정상화되었으며, CTX의 감소는 약물 투여 1주일 이후부터 나타나기 시작하여 1년까지 감소된 상태가 유지됨을 보여주었다. Padhi 등11)은 로모소주맙을 피하주사하였을 때 일주일 내에 혈장 내 약물 농도가 최대치로 증가하고, 이후에는 6–7일, 11–18일 두 번의 반감기로 감소하는 경향을 보임을 보고하였다.
로모소주맙을 투여 받은 11%–33%가량의 환자들은 로모소주맙에 대한 항체를 가질 수 있다. 이것은 특히 고용량이 투여된 환자들에서 확인되었는데, 중화 항체가 관찰되는 경우는 거의 없었으며, 3상 임상 연구에서는 골다공증으로 로모소주맙을 투여 받은 폐경기 여성의 0.6%–0.7%에서만 중화 항체가 확인되었다. 이에 학계에서는 로모소주맙에 대한 항체가 약물의 약력학 및 역동학적 결과에 미치는 영향이 매우 미미할 것으로 판단하고 있다.8,10,11,12,13)
3. 로모소주맙의 임상 효과
419명의 골감소증이 있는 폐경기 여성을 대상으로 한 2상 임상 연구13)에서 로모소주맙을 1년간 투여하였을 때 요추와 고관절에서 유의한 수준의 골밀도 증가가 확인되었다. 이러한 결과는 용량 의존적으로 매달 210 mg을 투여하였을 때 가장 높았으며, 대조군, 알렌드로네이트, 테리파라타이드를 투여한 군과 비교하였을 때도 유의하게 높은 수준이었다.
대표적 3상 임상 연구 중 하나인 ARCH (Active-Controlled Fracture Study in Postmenopausal Women with Osteoporosis at High Risk) 연구9)에서는 골다공증이 있는 4,093명의 폐경기 여성을 대상으로 12개월간 210 mg의 로모소주맙을 피하주사한 군과 70 mg 알렌드로네이트를 경구투여한 후 두 약제의 효과를 비교하였다. 이 연구에서 로모소주맙을 투여 받은 군은 알렌드로네이트를 투여 받은 군에 비해 요추 및 고관절 모두에서 유의한 수준의 골밀도의 증가와 골형성 골표지자의 상승 및 골흡수 표지자의 저하 소견이 확인되었다. 로모소주맙을 투여 받은 군은 알렌드로네이트를 투여 받은 군에 비해서 37%의 척추 골절의 감소 효과가 확인되었다. 비척추 골절의 감소효과는 26%였으나 통계적 유의성은 없었다.
또 다른 3상 임상 연구인 FRAME (Fracture Study in Postmenopausal Women with Osteoporosis) 연구8)는 골다공증이 있는 7,180명의 여성을 대상으로 한 이중맹검 무작위 대조군 연구이다. 이 연구에서는 약물 투여 12개월 후 로모소주맙을 투여한 군에서 요추 및 고관절 모두 유의한 수준의 골밀도의 증가와 함께 골형성 표지자의 상승 및 골흡수 표지자의 저하 소견이 확인되었다. 로모소주맙을 투여한 군은 대조군에 비해서 척추골절의 발생빈도가 73%가량 감소한 것이 확인되었다. 비척추골절의 발생 위험은 대조군에 비해서 25%가량 감소하였으나 통계적 유의성이 없는 것으로 확인되었다. 하지만 사후분석에서 라틴계열의 환자들을 제외할 경우 비척추골절의 위험이 42%까지 감소하는 것이 확인되었다.
STRUCTURE (An Open-label Study to Evaluate the Effect of Treatment With Romosozumab or Teriparatide in Postmenopausal Women) 연구14)는 3상 무작위 개방 연구이며 436명의 골다공증이 있는 폐경기 여성을 대상으로 로모소주맙과 테리파라타이드의 효과를 비교 분석하였다. 이 연구에서 로모소주맙을 투여 받은 군은 요추의 골밀도가 약물 투여 12개월 후 9.8%로 상승하여 테리파라타이드를 투여 받은 군의 5.4%보다 유의하게 큰 상승 정도를 보여주었다. 특히 로모소주맙을 투여받은 군은 고관절의 골밀도가 2.9%로 상승하는 것을 보여 주었는데, 이것은 같은 골형성 촉진제인 테리파라타이드가 고관절의 골밀도를 상승시키지 못한다는 점에 로모소주맙의 장점을 보여준 연구라고 할 수 있겠다.
로모소주맙은 남성의 골다공증에 대해서도 효과를 보여주었다. 50세 이상의 골다공증이 있는 남성 환자 245명을 대상으로 한 BRIDGE (placebo-controlled double-blind study evaluating the efficacy and safety of romosozumab in treating men with osteoporosis) 연구10)는 3상 이중 맹검 무작위 대조군 연구로 약물 투여 12개월 후 로모소주맙을 투여한 군의 요추 및 고관절의 골밀도 증가가 각각 12.1%, 1.2%로 확인되어 대조군의 2.5%, –0.5%에 비해 유의한 상승이 확인되었다. 골표지자 검사에서도 유의한 수준의 P1NP 증가 및 CTX 감소를 보여 골형성 촉진 및 골흡수 감소의 이중 효과가 작용한다는 것을 보고하였다.
Schemitsch 등15)은 로모소주맙의 골형성효과가 고관절 골절 환자에서 임상 결과를 향상시킬 수 있는가에 대한 연구를 시행하였다. 그들은 332명의 대퇴골 전자간 골절 및 대퇴골 경부 골절 환자를 대상으로 이중 맹검 무작위 대조군 연구를 시행하였는데, 골절의 유합시간 및 임상결과에서 두 군 간에 유의한 차이를 확인할 수 없었다고 보고하였다.
4. 로모소주맙의 안전성
현재까지 보고된 임상 연구에서 로모소주맙은 비교적 안전한 약물로 받아들여지고 있다. 210 mg 로모소주맙을 피하주사하였을 때 주사 부위의 이상 반응이 4.4%–5.2%에서 보고되었으나 대조군이 2.6%–2.9%임을 감안하면 임상적으로 큰 문제가 되지는 않을 것으로 보인다.8,9) 1상 임상 시험 중 혈중 transaminase의 상승이 있는 1명의 환자가 확인되었으나 간기능의 변화를 초래하지는 않았으며, 2상 임상 시험에서는 고용량을 사용한 환자에서 간헐적인 부갑상선호르몬 및 칼슘 농도의 상승이 확인되었으나 관련 증상이 없거나 경미한 수준이었다.11,13) 로모소주맙을 투여한 후 1년간 15%–20%의 환자에서 로모소주맙에 대한 항체가 확인되었으나 이 항체가 약물 치료의 효과나 안정성에 영향을 준다는 증거는 없으며, 항체의 역가와 주사 부위 이상 반응 혹은 다른 부작용과 연관성도 확인되지 않았다.8,9,10,13)
Wint 신호체계는 다양한 조직에서 세포증식과 관련이 된 것으로 알려져 있기 때문에 항 sclerostin 치료에 의한 악성 종양의 발생가능성에 대한 우려가 있을 수 있다. 그러나 쥐를 대상으로 한 연구에서 로모소주맙의 치료와 관련된 악성 종양의 발생 빈도 증가는 확인되지 않았으며, 이것은 테리파라타이드나 abaloparatide와 같은 골형성 효과가 있는 약물에서 용량 의존적으로 악성 골육종의 유도가 가능하였던 연구와 다른 결과를 보여주었다.16,17,18)
로모소주맙에 의한 심혈관계 부작용의 발생 가능성은 비교적 낮은 것으로 보고되고 있다. FRAME 연구8)에서 보고되는 약물 투여 후 심혈관계 질환의 발생 빈도는 1.2%로 대조군의 1.1%와 거의 같은 수준이며 사망발생 빈도도 로모소주맙이 0.8%, 대조군이 0.6%로 확인되었다. 한편 ARCH 연구9)에서는 약물 투여 12개월 뒤 심혈관계 질환 및 뇌졸중의 발생빈도가 0.8%로 알렌드로네이트의 0.3%에 비해서 높게 확인되었고, 사망발생 빈도도 1.5%로 알렌드로네이트의 1.0%에 비해서 높게 확인되었다. 그러나 이러한 심혈관계 합병증의 발생과 관련한 로모소주맙의 작용기전에 대해서는 알려진 바가 없다.
5. 로모소주맙의 임상 적용
2020년 미국임상내분비학회/내분비학회(American Association of Clinical Endocrinology/American College of Endocrinology, AACE/ACE)에서는 다발성 척추 골절이 있으면서 고관절이나 척추의 골밀도 T-점수가 −2.5 이하인 경우를 골다공증 골절의 초고위험군으로 새롭게 정의하고 이러한 환자군에서는 초기 치료부터 골절 예방을 위한 강력한 약물치료를 권고하였다. 이러한 경우에는 로모소주맙을 일차 약제로 선택해야 하며, 칼슘과 비타민 D의 보충과 함께 210 mg 로모소주맙(105 mg씩 연속 두 번 다른 부위에 피하주사)을 1년간 매달 피하주사할 것을 권장하고 있다. 단, 심혈관계 질환이나 뇌졸중이 있는 환자, 심근 경색이 있었던 환자에서는 이 약제와 심혈관계 질환의 관련성에 대한 연구가 더 이루어질 때까지 사용을 보류하는 것이 좋겠다고 언급하고 있다.19)
기존의 비스포스포네이트나 데노수맙과 같은 골흡수 억제제를 사용하였던 환자들에서 골밀도의 증가나 골표지자의 변화가 최소 유의변화(least significant change, LCS) 이상으로 변화되지 않거나 새로운 골절이 발생하는 경우는 기존 약제의 무반응자(non-responder)로 판단할 수 있다. 이러한 경우에는 골형성 촉진제로의 변환이 필요한데 이 경우 역시 로모소주맙 사용의 적응이 될 수 있다.19)
한국에서는 2020년 12월부터 로모소주맙에 대한 급여를 적용하고 있다. 하지만 기존 비스포스포네이트 제제 중 한 가지 이상에 효과가 없거나, 비스포스포네이트를 사용할 수 없는 65세 이상의 폐경 후 여성 중 이중 에너지 방사선 흡수계측(dual energy X-ray absorptiometry, DEXA)에서 중심골 (요추 및 대퇴골) 골밀도 T-점수가 −2.5 이하이고 골다공증 골절이 2개 이상 발생한 환자의 경우로 제한을 두고 있어 아직 많은 환자들이 급여 적용을 받기 어려운 실정이다.
로모소주맙은 비스포스포네이트와 달리 약물의 지속 효과가 없다. 따라서 치료를 중단하는 경우 약물의 효과는 가역적이기 때문에 다른 골다공증 약제로 전환하여 치료를 지속해야 한다. FRAME 연구8)와 이후 데노수맙을 추가로 2년 더 연장하여 투여한 FRAME Extension 연구20)에서 로모소주맙과 데노수맙을 순차적으로 사용한 군에서 약물 투여 2년 후의 골밀도의 증가가 대조군에 비해 유의하게 증가하였고 이러한 차이가 3년까지 유지됨을 확인하였다. 데노수맙으로 전환한 2년 후의 골절 예방 효과는 척추 골절이 66%, 비척추 골절이 21%로 확인되었다.21) ARCH 연구9)에서도 로모소주맙 투여 이후 비스포스포네이트로 전환 투여 하였을 때 로모소주맙의 투여로 인한 골밀도의 상승과 척추골절 및 비척추 골절의 예방효과가 유지됨이 확인되었다. 이러한 결과를 바탕으로 로모소주맙의 투여를 중단하는 경우에는 데노수맙이나 비스포스포네이트로 전환하여 골다공증 치료를 지속하는 것을 권장한다.
결 론
그간의 연구에서 골밀도의 증가, 골절 예방에 대한 로모소주맙의 우수한 효과가 보고되고 있다. 골형성 촉진, 골흡수 억제 등의 이중 작용을 통해 기존 골다공증 치료제의 부족한 점을 보완하고, 특히 치료에 반응하지 않는 경우와 초고위험군에서의 치료에 더 나은 결과를 기대하고 있다. 그러나 아직임상 효과, 안전성 등에 대한 결과가 충분하지 않은 실정으로 이에 대한 지속적인 추가 연구가 필요할 것으로 생각된다.
Financial support:None.
Conflict of interests:None.
Acknowledgements
This work was supported by clinical research grant in 2021 from Pusan National University Hospital.

 E-submission
E-submission KOTA
KOTA TOTA
TOTA TOTS
TOTS


 Cite
Cite